les constituants de la matière
|
La matière est la substance qui compose tout corps ayant une réalité tangible.
Ses trois états les plus communs sont l'état solide, l'état liquide, l'état gazeux. Elle occupe de l'espace et la quantité de matière se mesure à l'aide de la masse. Lorsqu'il s'agit de compter des particules de matière, on utilise la mole. |
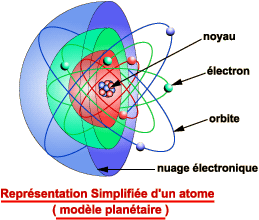
Un atome est la plus petite partie d'un corps simple pouvant se combiner chimiquement avec une autre. Chaque atome a un nom et un symbole qui lui sont propres.
Le diamètre d'un atome est de l'ordre de 10^-10 m. Il est constitué d'un noyau composé de protons et de neutrons autour desquels orbitent des électrons. Le diamètre d'un noyau est de l'ordre de 10^-15 m Loin du noyau se trouve le nuage électronique. Un atome est électriquement neutre. Il possédera autant d'électrons négatifs dans le nuage électronique que de protons positifs dans le noyau.. |
|
Tous les atomes de même numéro atomique Z ont le même nom et le même symbole : ils appartiennent au même élément. On les appelle des isotopes.
Un élément est donc caractérisé par son symbole et son numéro atomique Z. Tous les atomes existants sont recensés dans le tableau périodique. |
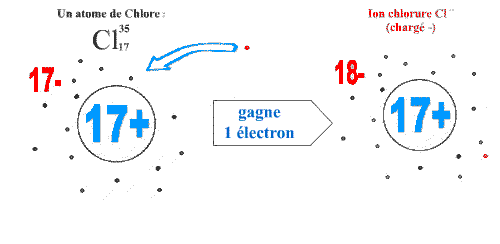
Ex : l'atome de chlore le plus abondant dans la nature possède un noyau central contenant Z = 17 protons positifs et N = 18 neutrons. Le nombre de nucléons est donc A = Z + N = 17 + 18 = 35. Z = 17 est également appelé le numéro atomique. C'est le numéro de la case du tableau périodique des éléments dans laquelle se trouve le chlore.
L'atome de chlore possédant 17 protons positifs dans le noyau aura donc 17 électrons négatif répartis sur trois couches : (K)2, (L)8, (M)7, loin du noyau. |
Mendéléïev (1834-1907) eut l'idée de classer les éléments, connus à son époque, en colonnes et en lignes par ordre de masses molaires atomiques croissantes, de telle manière que les éléments figurant dans une même colonne présentent des propriétés chimiques semblables. C'est la classification périodique des éléments. Elle comporte 7 lignes (ou périodes) et 18 colonnes.
Critères de classement :
Critères de classement :
- Les atomes sont classés sur chaque par ordre croissant du numéro atomique Z.
- Sur une même ligne, les atomes des éléments ont la même couche externe :
Ligne 1 : Couche K // Ligne 2 : Couche L // Ligne 3 : Couche M
Un élément de la 3e ligne possède 3 couches d'électrons. - Dans une même colonne, les atomes des éléments ont le même nombre d'électrons sur leur couche externe, qui correspond au numéro de la colonne (sauf pour He)
Un élément de la 7e colonne possède 7 électrons sur sa couche externe.
Les éléments de la dernière colonne constitue la famille des gaz rares (ou gaz inertes). Ils ont leur couche externe saturée.
He : (K)2 ; Ne : (K)2 (L)8 ...
Ces gaz nobles sont stables. Ils sont les seuls atomes pouvant exister isolés.
Lors de transformations chimiques, les atomes évoluent pour acquérir la structure électronique du gaz noble le plus proche d'eux dans le tableau périodique. Ils acquièrent ainsi une plus grande stabilité. Ils obéissent soit à la règle du duet, soit à la règle de l'octet.
Règle du duet : Les atomes proches de l'hélium évoluent pour acquérir deux électrons externes.
Règle de l'octet : Les autres atomes évoluent pour acquérir huit électrons sur leur couche externe.
Ces évolutions aboutissent à des molécules ou à des ions.
He : (K)2 ; Ne : (K)2 (L)8 ...
Ces gaz nobles sont stables. Ils sont les seuls atomes pouvant exister isolés.
Lors de transformations chimiques, les atomes évoluent pour acquérir la structure électronique du gaz noble le plus proche d'eux dans le tableau périodique. Ils acquièrent ainsi une plus grande stabilité. Ils obéissent soit à la règle du duet, soit à la règle de l'octet.
Règle du duet : Les atomes proches de l'hélium évoluent pour acquérir deux électrons externes.
Règle de l'octet : Les autres atomes évoluent pour acquérir huit électrons sur leur couche externe.
Ces évolutions aboutissent à des molécules ou à des ions.
|
Molécule : Ensemble d'atomes unis les uns aux autres par des liaisons chimiques. C'est un assemblage chimique électriquement neutre, qui peut exister à l'état libre, et qui représente la plus petite quantité de matière possédant les propriétés caractéristiques de la substance considérée.
Les molécules sont représentées de diverses façons, selon l'objectif attendu. Liaison covalente : Liaison entre deux atomes, résultant de la mise en commun de deux électrons. Ion : Atome, ou groupement d'atomes chargés :
Négativement = aNions (excès d'électrons) positivement = cations (déficit en électrons) |
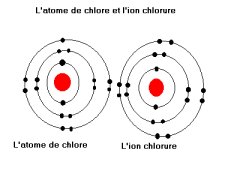
Ex : Cl : (K)2, (L)8, (M)7 = il manque 1 électron sur la couche externe.
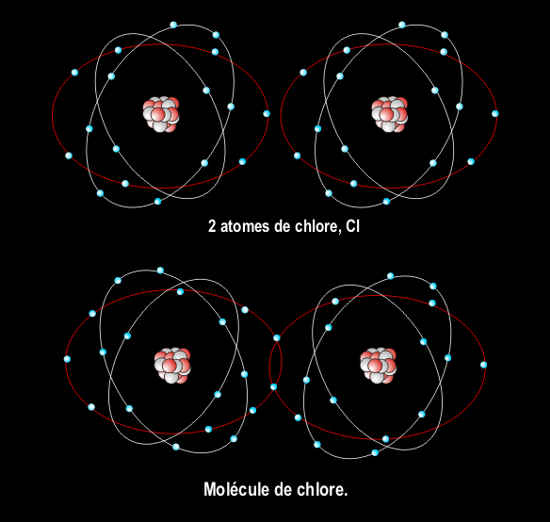
2 atomes de Cl : chacun peut mettre un électron en commun, la molécule de Cl2 est stable. L’ion Cl- est stable. |
mesurer la matière : masse et quantité de matière
|
Quantité = nombre n
La mole (unité : mol) = quantité de matière d’un système contenant autant d'entités élémentaires qu'il y a d'atomes dans 12 grammes de carbone 12. Une mole d’atomes contient environ 6,022 × 10^23 atomes. Ce nombre est appelé nombre d'Avogadro. La mole est une unité de comptage au même titre que la centaine, la vingtaine ou la douzaine, sauf que cette unité de comptage est immense (environ 602 200 milliards de milliards d'unités). |
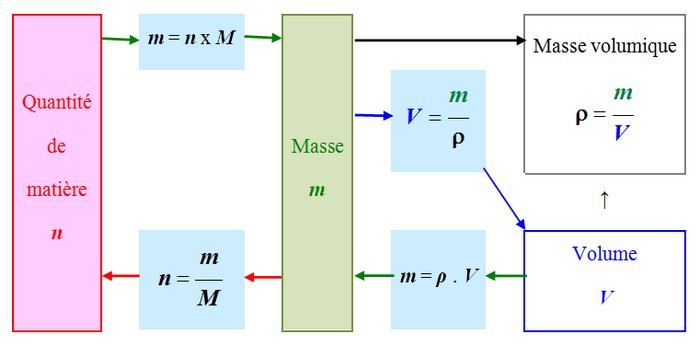
La masse molaire M est la masse d'une mole d'une substance (un corps simple, un composé chimique). Elle s'exprime en grammes par mole.
Masse molaire d’un élément : masse d’une mole d’atomes pris dans les proportions isotopiques naturelles. Ex : le chlore est un mélange de deux isotopes, M(Cl) = 35,5 g/mol Masse molaire moléculaire : somme des masses molaires des éléments (tableau périodique). Masse molaire d'un composé ionique : la masse des électrons est négligeable par rapport à la masse des nucléons présents dans les noyaux. |
mesurer la matière en solution : concentrations
|
Solution : mélange homogène d'au moins deux substances
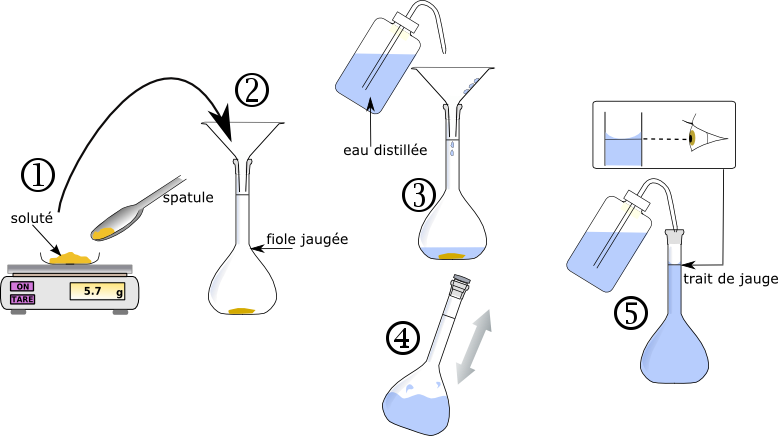
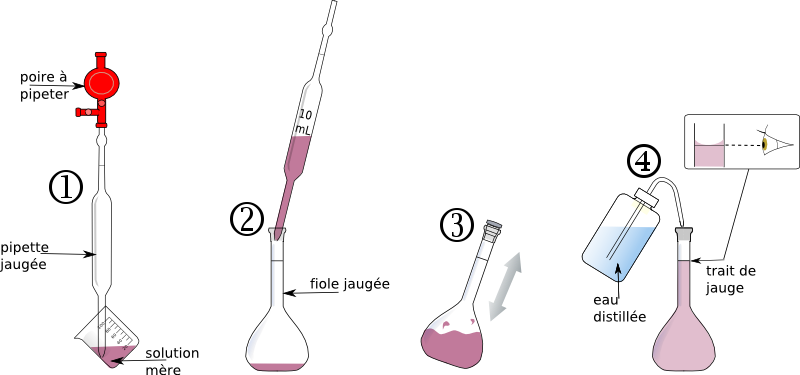
Solvant : substance en plus grande quantité Soluté : substance en plus faible quantité, dissoute dans le solvant. Solution aqueuse : solvant = eau, soluté = gaz ou liquide Solution ionique : ions en solution dans de l'eau préparation d'une solution : par dissolution ou dilution. |
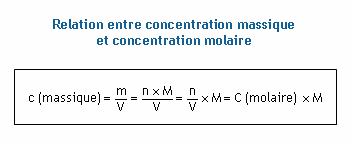
Concentration : proportion, part d’une substance dans un mélange.
Concentration molaire C (mol/L) Concentration massique Cm = titre massique t (g/L) |
unités spécifiques à l'analyse d'eau :
Electroneutralité : une solution est toujours neutre, il y a autant de charges positives que de charges négatives.
En analyse d'eau, on s'intéresse souvent uniquement aux charges portées par les ions en solution.
Milli-équivalent (mé) : 1 mé = 1 mmol de charges électriques élémentaires.
Degré Français : 1 mé/L = 5 °F ou 1 °F = 0,2 mé/L
Cette unité de concentration ne s’applique plus guère qu’aux «titres» tels que le titre alcalin, le titre hydrotimétrique....
Electroneutralité : une solution est toujours neutre, il y a autant de charges positives que de charges négatives.
En analyse d'eau, on s'intéresse souvent uniquement aux charges portées par les ions en solution.
Milli-équivalent (mé) : 1 mé = 1 mmol de charges électriques élémentaires.
Degré Français : 1 mé/L = 5 °F ou 1 °F = 0,2 mé/L
Cette unité de concentration ne s’applique plus guère qu’aux «titres» tels que le titre alcalin, le titre hydrotimétrique....