|
|
4.1 structure des molécules et des ions
Les électrons de la couche externe d'un atome sont appelés électrons de valence. Les atomes tendent à adopter la structure électronique stable du gaz noble le plus proche, c'est à dire à posséder 2 électrons de valence (règle du duet) ou 8 (règle de l'octet).
Les électrons de valence d'une molécule sont les électrons de valence des atomes qui la constituent.
Les ions sont des atomes ou des molécules ayant gagné ou perdu un ou plusieurs électrons pour respecter la règle du duet ou de l'octet. Anion : chargé négativement et cation : chargé positivement.
Pour former une molécule, les atomes s'associent en formant des liaisons covalentes. Une liaison covalente est formée par un doublet liant résultant de la mise en commun de deux électrons fournis par chacun des atomes liés.
Cette liaison est représentée par un trait entre les deux atomes liés.
Les électrons de valence non engagés dans les liaisons covalentes sont regroupés en doublets non liants.
Dans la représentation de Lewis d'une molécule, toutes les liaisons covalentes et touts le doublets non-liants sont représentés.
La géométrie d'une molécule peut être prévue à partir de sa formule de Lewis : les doublets (liants et non liants) vont s'éloigner au maximum les uns des autres autour d'un atome.
les molécules de la chimie organique sont composées essentiellement d’atomes de carbone et d’hydrogène, et dans une moindre mesure d’atomes d’oxygène et d’azote.
l’enchaînement des atomes de carbone constituant une molécule organique forme une chaine carbonée
Les électrons de valence d'une molécule sont les électrons de valence des atomes qui la constituent.
Les ions sont des atomes ou des molécules ayant gagné ou perdu un ou plusieurs électrons pour respecter la règle du duet ou de l'octet. Anion : chargé négativement et cation : chargé positivement.
Pour former une molécule, les atomes s'associent en formant des liaisons covalentes. Une liaison covalente est formée par un doublet liant résultant de la mise en commun de deux électrons fournis par chacun des atomes liés.
Cette liaison est représentée par un trait entre les deux atomes liés.
Les électrons de valence non engagés dans les liaisons covalentes sont regroupés en doublets non liants.
Dans la représentation de Lewis d'une molécule, toutes les liaisons covalentes et touts le doublets non-liants sont représentés.
La géométrie d'une molécule peut être prévue à partir de sa formule de Lewis : les doublets (liants et non liants) vont s'éloigner au maximum les uns des autres autour d'un atome.
les molécules de la chimie organique sont composées essentiellement d’atomes de carbone et d’hydrogène, et dans une moindre mesure d’atomes d’oxygène et d’azote.
l’enchaînement des atomes de carbone constituant une molécule organique forme une chaine carbonée
4.2 géométrie des entités
|
|
|
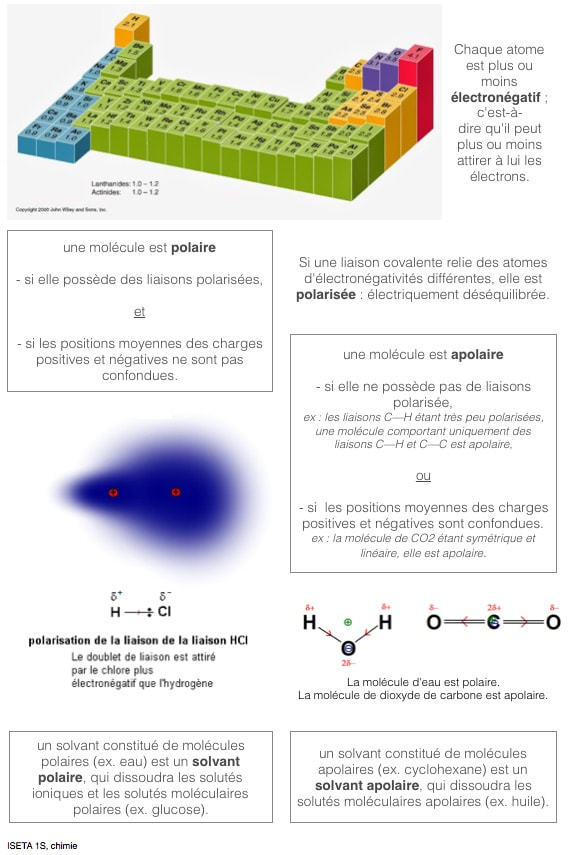
4.3 polarité d'une molécule
|
Tout les atomes sont plus ou moins électronégatif ; c'est-à-dire qu'ils peuvent plus ou moins attirer à eux les électrons.
Si une liaison covalente relie des atomes d'électronégativités différentes, elle est polarisée : électriquement déséquilibrée. une molécule est polaire si elle possède des liaisons polarisées, et si les positions moyennes des charges positives et négatives ne sont pas confondues. une molécule est apolaire si l’une de ces deux conditions n’est pas vérifiée. Les liaisons C—H étant très peu polarisées, une molécule comportant uniquement des liaisons C—H et C—C est apolaire. |