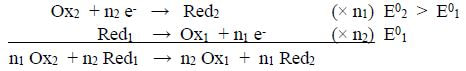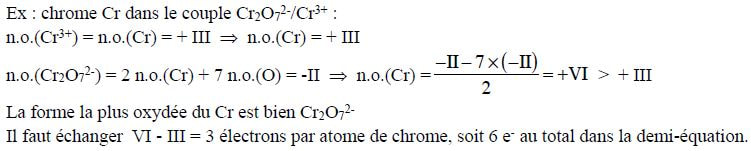vocabulaire
|
oxydant : espèce chimique capable de capter un ou plusieurs électrons.
ex : Cu2+ + 2 e- → Cu L’ion cuivre II (oxydant) est réduit en métal cuivre (réducteur) ; c’est une réduction (= gain d’électrons) réducteur : espèce chimique capable de céder un ou plusieurs électrons.
ex : Zn → Zn2+ + 2e - Le métal zinc (réducteur) est oxydé en ion zinc (oxydant) ; c’est une oxydation (= perte d’électrons) |
couple : ensemble formé par la forme oxydée et la forme réduite du même élément chimique
noté par convention Ox / Red. ex : Cu2+/Cu ; Zn2+/Zn demi-équation électronique : traduit le lien entre la forme oxydée et la forme réduite de l’élément.
|
réaction
|
une réaction d’oxydoréduction est un transfert d'électron(s) entre la forme oxydée d’un couple et la forme réduite d’un autre couple
|
une réaction d'oxydoréduction est une réaction chimique au cours de laquelle :
- les éléments chimiques et la charge électrique se conservent dans chaque demi-équation, - TOUS les électrons cédés par le réducteur d’un couple sont captés par l’oxydant de l’autre couple. |
|
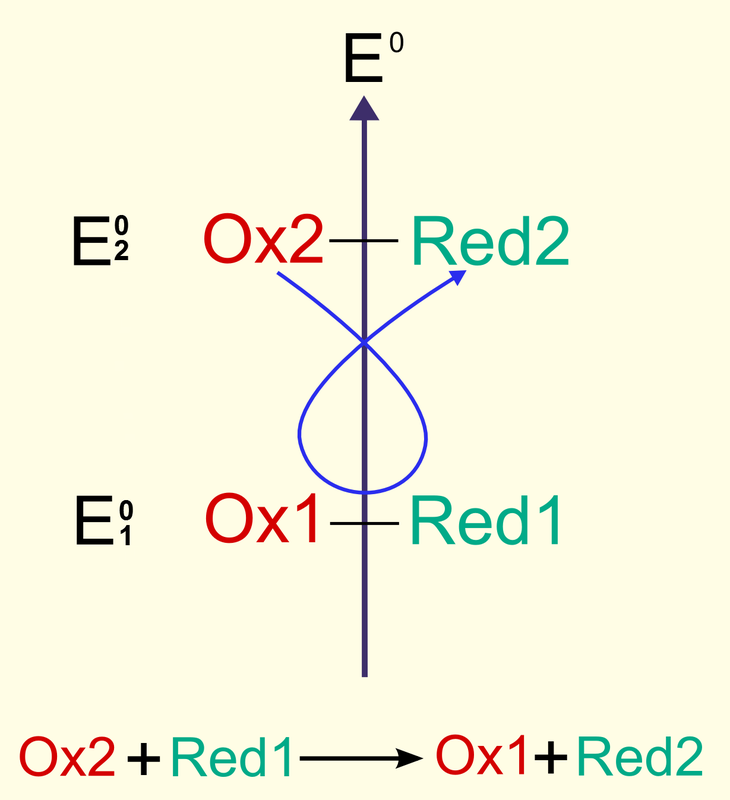
règle du gamma :
les couples redox peuvent être classés selon la « force » de leur oxydant (= capacité à capter des électrons plus ou moins facilement, quantifiée par le potentiel redox standard E0). plus fort est l’oxydant, plus son réducteur conjugué est faible. plus l'oxydant d'un couple est fort, plus le potentiel E0 de ce couple est élevé. entre deux couples rédox, une seule réaction peut se produire spontanément : celle de l’oxydant le plus fort sur le réducteur le plus fort. |
nombre d'oxydation
|
en chimie, l'état d'oxydation, décrit par le nombre d'oxydation (n.o.), est un concept servant à caractériser l'état électronique d'un atome dans une espèce chimique par rapport à l'état élémentaire neutre servant de référence (n.o. = 0).
on note ce nombre en chiffres romains. |
calcul :
n.o. (espèce) = Σ n.o. (atomes dans l’espèce) = charge (espèce)
dans la plupart des composés, n.o.(O) = -II n.o.(H) = + I |
utilisations :
|
reconnaître une réaction d'oxydoréduction
si, au cours d'une réaction, on n'observe aucune variation des n.o. des éléments, cette réaction n'est pas une réaction d'oxydo-réduction. identifier la forme la plus oxydée d'un élément chimique
n.o.(Ox) > n.o.(Red). |
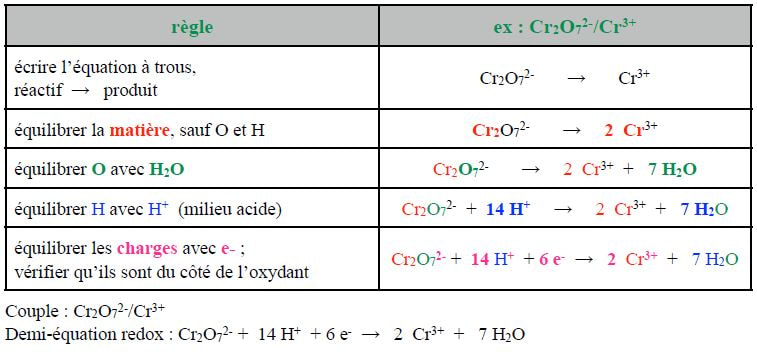
équilibrer une réaction d'oxydoréduction
La variation globale de n.o. est nulle lors d'une réaction redox. déterminer le nombre d'électrons en jeu dans une demi-équation électronique
n.o.(Ox) – n.o.(Red) = nb e- échangés par atome de l'élément. |