lumière et couleur
|
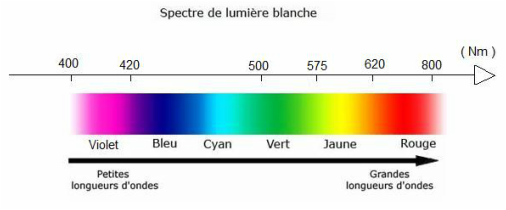
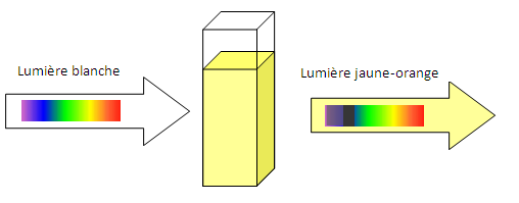
s La lumière blanche est une lumière polychromatique.
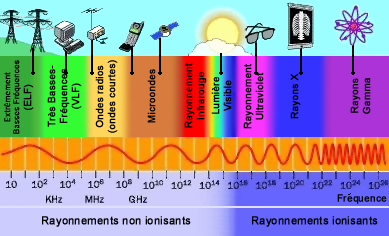
Elle comporte toutes les longueurs d’onde comprises entre 400 et 800 nm. La lumière fait partie de l’ensemble du rayonnement électromagnétique. Le rayonnement électromagnétique est l’une des formes de l’énergie. C’est une onde, c’est à dire un phénomène ondulatoire, caractérisé par une vitesse de propagation c = 3 x 10^8 m/s, une fréquence ν (Hz) et une longueur d’onde λ (m). Cette onde est associée à un corpuscule, le photon, d’énergie E (J), avec la constante de Planck h = 6,67 x 10^-34 J.s \( c = \lambda \times \nu \) et \( E = h \times \nu = \frac{h \times c}{\lambda} \) |
|
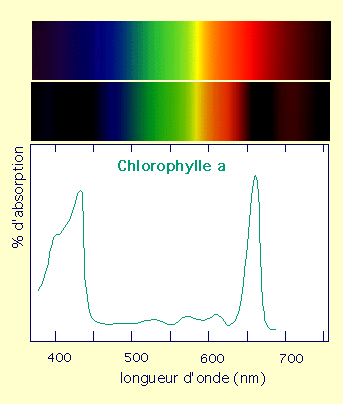
Une solution est colorée si elle absorbe une partie des radiations de la lumière blanche. Sa couleur est constituée des radiations qui l’ont traversée.
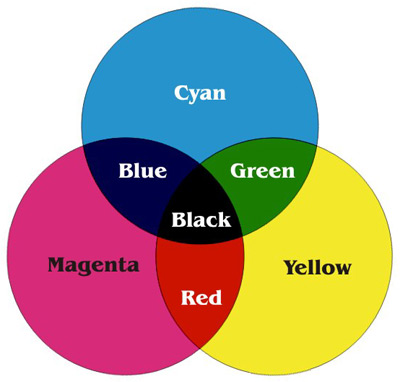
Ex la chlorophylle : elle absorbe le rayonnement rouge et le bleu (= magenta ; l’énergie correspondante permet la photosynthèse) et n’utilise pas le vert. |
spectrophotométrie
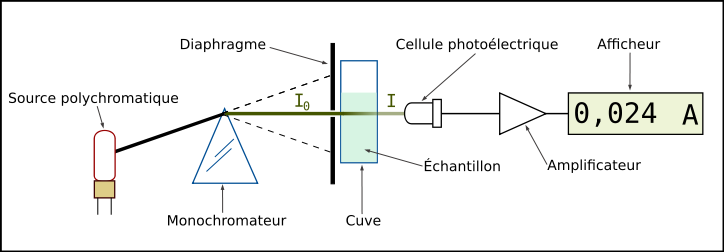
Lorsqu'un faisceau de lumière monochromatique traverse un milieu absorbant, l'intensité du faisceau transmis est inférieure à l'intensité du faisceau incident.
Absorbance de la solution A : elle caractérise l'absorption de l’intensité lumineuse à travers une substance.
Absorbance de la solution A : elle caractérise l'absorption de l’intensité lumineuse à travers une substance.
Loi de Beer-Lambert : l’absorbance d’une solution est proportionnelle à la concentration de l‘espèce chimique responsable de l’absorption (à la longueur d’onde utilisée) :
A = ε x l x C
A : absorbance, sans unité
C : concentration de l’espèce en mol/L
ε : coefficient d’extinction molaire de l'espèce absorbante, en L/(mol.cm)
l : longueur traversée de la cuve en cm
L'absorbance est une grandeur additive : si deux substances absorbantes sont présentes dans la même solution aux concentrations respectives C1et C2, l'absorbance mesurée à la longueur d'onde λ est la somme des absorbances.
A = ε x l x C
A : absorbance, sans unité
C : concentration de l’espèce en mol/L
ε : coefficient d’extinction molaire de l'espèce absorbante, en L/(mol.cm)
l : longueur traversée de la cuve en cm
L'absorbance est une grandeur additive : si deux substances absorbantes sont présentes dans la même solution aux concentrations respectives C1et C2, l'absorbance mesurée à la longueur d'onde λ est la somme des absorbances.
|
Mesure
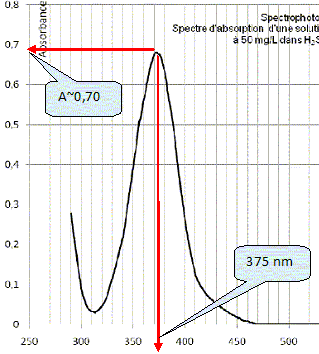
On obtient la courbe d’absorption (= spectre d’absorption).
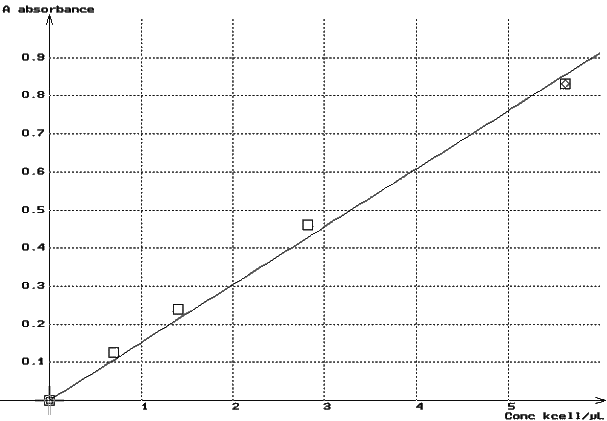
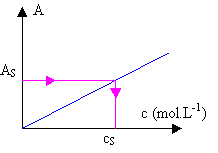
On obtient une droite passant par l’origine : les deux grandeurs sont proportionnelles, la loi de Beer-Lambert est bien vérifiée.
On peut suivre l'évolution au cours du temps de l'absorbance d'une solution. |
|
Utilisation en analyse d'eau
Principalement les composés azotés (NH4+, NO3-, NO2-) et phosphorés (phosphates) Principe : faire réagir le composé recherché avec un réactif en excès pour obtenir un produit coloré. L'appareil est pré-calibré et programmé : λmax et la courbe d’étalonnage sont enregistrées pour chaque espèce chimique recherchée. Il faut juste suivre le protocole :
|