liste des paramètres présentés
|
alcalinité
nitrates phosphates |
dureté
nitrites |
dioxygène dissous
ammonium |
paramètres généraux
alcalinité TA-TACLe terme « alcalin » désigne un élément qui a les propriétés d’une base : l’alcalinité correspond à la quantité d’acide qui peut être captée par les ions présents dans l’eau.
L’alcalinité d'une eau exprime sa teneur en anions : hydroxyde, carbonate, hydrogénocarbonate = bicarbonate, phosphate, silicate ... Ces ions sont liés principalement à des ions alcalins (Na+, K+) ou alcalino-terreux (Ca2+, Mg2+).
nitratesToutes les formes d’azote sont susceptibles d’être à l’origine des nitrates par oxydation biologique.
Les nitrates proviennent : - du lessivage des engrais, - de l'azote reminéralisé sur les zones de culture, - des eaux usées domestiques, - et parfois des eaux usées industrielles. Les nitrates sont très lessivables, ils ne sont pas retenus dans les sols par le complexe argilo-humique. Ils constituent l'un des éléments nutritifs majeurs des végétaux. Les nitrates participent à la croissance des végétaux dans l'eau, étouffant les autres organismes vivants et provoquant ce que l'on appelle un phénomène d'eutrophisation. Ils constituent donc un danger pour la faune et la flore lorsqu'ils sont présents en quantité trop importante. Les nitrates n’ont pas d’effet toxique direct, mais ils peuvent donner naissance chez les nourrissons à des nitrites toxiques (formation de méthémoglobine). phosphatesLe phosphore peut se trouver sous différentes formes oxydées.
Les phosphates font partie des anions facilement fixés par le sol. Leur présence dans les eaux naturelles est liée à la nature des terrains traversés et à la décomposition de la matière organique. Bien que dans le sol les formes prédominantes du phosphore soient H2PO4-, HPO42-, on désigne, pour simplifier, les anions phosphoriques par PO43-. C'est d'ailleurs sous cette forme que la plante absorbe le phosphore. Les sédiments fixent l’essentiel du phosphore ; en conditions anaérobies, les ions phosphates sont libérés. En milieu aqueux, les acides métaphosphorique (HPO3) et pyrophosphorique (H4P2O7) tendent vers une forme plus stable : l’orthophosphate P2O5. Pratiquement, c’est sous cette forme qu’on le rencontre dans des eaux superficielles dont le pH est compris entre 5 et 8. Origine : - minérale : les anions « phosphoriques » H2PO4-, HPO42-, PO43- provenant des engrais, de la décomposition des roches, des eaux industrielles, des adjuvants ajoutés aux détergents... - organique : les humophosphates provenant de la dégradation des substances animales ou végétales (purin, fumier, fosse d'aisance...). Rejets industriels (l'activité industrielle participe pour environ 25% aux rejets dans l'eau de phosphore : agro-alimentaire, laveries…) et domestiques (eaux usées), ou lessivage des terres cultivées (engrais, certains pesticides). Ils proviennent aussi des eaux industrielles traitées contre la corrosion ou des eaux domestiques : ils servent à diminuer la dureté de l’eau, facilitent l’émulsion des lipides et maintiennent les salissures dans l’eau. Les phosphates échappent en majeur partie (80%) au traitement des stations d’épuration aérobies biologiques classiques. Par ailleurs, les détergents génèrent la formation de mousses dans les égouts, la STEP et le milieu naturel. Le phosphore joue un rôle important dans le développement des algues : il est considéré que 1 mg de phosphore peut contribuer à l’élaboration de 70 à 80 mg de matière organique. Les eaux contenant des phosphates en excès présentent une grande fertilité. Il s'en suit un développement important de phytoplancton (algues bleues) en surface et une accumulation en plantes au fond des réservoirs aquatiques. La transparence de l'eau diminue, la photosynthèse est ralentie, la décomposition de la matière végétale consomme le dioxygène dissous, il se forme des produits toxiques tels que H2S et NH3. La faune et la flore disparaissent c'est le stade ultime de l'eutrophisation synonyme de mort biologique du milieu. En eaux courantes (rivières) la pollution par les phosphates concerne l’ensemble du réseau hydrographique ; cependant les excès de végétation, témoins de cette pollution, ne touchent que les zones suffisamment calmes pour permettre aux algues et herbiers de proliférer. Les milieux de grande taille ayant reçu depuis longtemps d’importantes quantités de phosphore mises en mémoire dans les sédiments sont difficilement récupérables. |
dureté THLa dureté d'une eau exprime sa teneur en métaux alcalino-terreux (2nde colonne de la classification périodique des éléments, qui donnent des cations de valence 2) : essentiellement en ions calcium et magnésium dissous dans l'eau sous forme de :
carbonates (peu solubles, CaCO3, MgCO3), bicarbonates ou hydrogénocarbonates (solubles, Ca(HCO3)2), chlorures, sulfates... Sauf exceptions très particulières, la dureté a un caractère naturel lié au lessivage des terrains traversés, et correspond à la teneurs en ions calcium et magnésium. Les eaux provenant de terrains calcaires et surtout de terrains gypseux peuvent avoir des duretés très élevées susceptibles d'atteindre 1 g/L de CaCO3. Par contre, les eaux en provenance de terrains cristallins, métamorphiques ou schisteux auront des duretés très faibles.
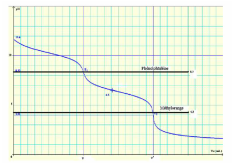
Dureté totale TH = dureté calcique + dureté magnésienne Les sels de calcium et de magnésium précipitent avec le savon, qui perd ainsi son pouvoir détersif, et ne mousse plus. Des eaux dures peuvent, dans certaines conditions de pH et de température, former des dépôts de carbonates et entartrer les canalisations. Par contre, une faible dureté ne permet pas l’élaboration d’une couche carbonatée assurant le plus souvent une protection des canalisations contre certains risques de corrosion. nitritesOrigine : oxydation incomplète de l’ammoniaque, ou réduction des nitrates.
Une eau qui contient de nitrites est à considérer comme suspecte, mais il faut tenir compte des teneurs en nitrates, azote ammoniacal, matières organiques et de l’examen bactériologique. La forme moléculaire HNO2 (acide nitreux) est plus toxique que l’ion NO2-. Leur toxicité est très significative (pouvoir oxydant) + action méthémoglobinisante. Ils peuvent être transformés en nitrosamines, cancérigènes. |
dioxygène dissousLe dioxygène, toujours présent dans l’eau, n’en est pas un élément constitutif. Sa solubilité est fonction de la température, de la pression partielle dans l’atmosphère et de la salinité (cf loi de Henry).
Il conserve ses propriétés oxydantes. Les variations de la teneur en dioxygène sont aussi importantes que la valeur du taux absolu. Elles peuvent être fonction de la présence de végétaux, de matières organiques oxydables, d’organismes aérobies, de perturbations des échanges à l’interface eau-atmosphère (ex : hydrocarbures, détergents), du moment de la journée ... La concentration en O2 d’une eau peut donner lieu à diverses interprétations :
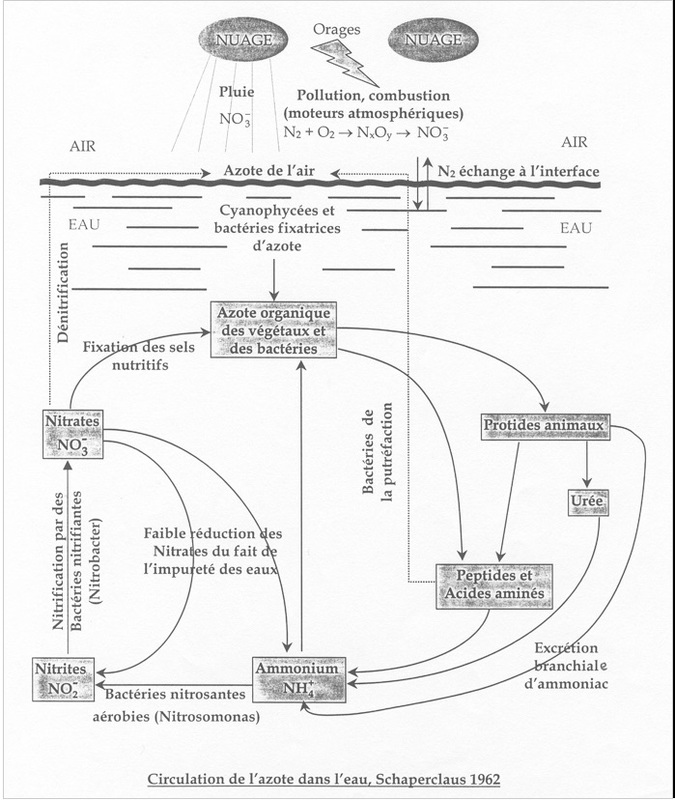
ammoniumTraduit habituellement un processus de dégradation incomplète de la matière organique.
Origines : matière végétale des cours d’eau, matière organique animale ou humaine, rejets industriels, engrais… Le brassage des vases des cours d’eau peut entraîner la libération d’eaux interstitielles très riches en ammoniaque. L’ammoniac est très soluble dans l’eau. En général, l’ammoniaque se transforme assez rapidement en nitrites et nitrates par oxydation biologique. C’est la forme non ionisée, NH3 (ammoniac) qui est toxique pour les poissons, en empêchant l’oxydation de l’hémoglobine. Sa proportion par rapport à la forme non toxique ionisée NH4+ (ion ammonium) dépend du pH et de la température. L’élévation de température, les faibles teneurs en CO2 et en O2 accroissent la toxicité. Pour un pH > 8,5 la forme toxique est majoritaire. |