5.1 cohésion dans un solide
|
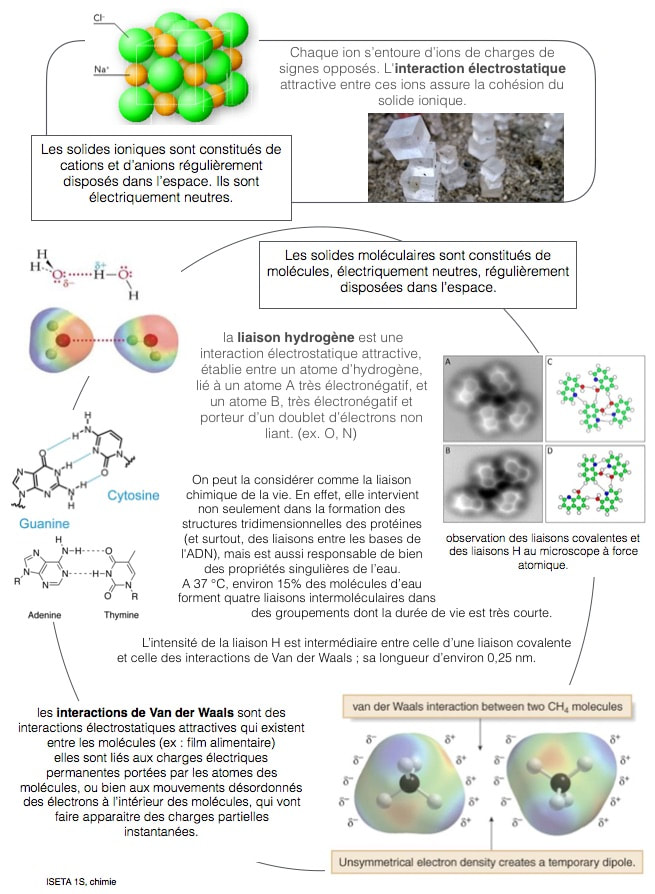
Les solides ioniques sont constitués de cation et d’anions régulièrement disposés dans l’espace. Ils sont électriquement neutres.
Dans un solide ionique, chaque ion s’entoure d’ions de charges de signes opposés. L'interaction électrostatique attractive entre ces ions assure la cohésion du solide ionique. la formule du solide ionique indique la proportion d’anions et de cations nécessaires pour assurer la neutralité électrique Les solides moléculaires sont constitués de molécules, électriquement neutres, régulièrement disposées dans l’espace la cohésion d’un solide moléculaire est due aux interactions de Van der Waals, qui sont toujours présentes, et aux liaisons hydrogène lorsqu'elles existent. une liaison hydrogène est une interaction électrostatique attractive, établie entre un atome d’hydrogène, lié à un atome A très électronégatif, et un atome B, très électronégatif et porteur d’un doublet d’électrons non liant. (ex. eau solide)
les interactions de Van der Waals sont des interactions électrostatiques attractives qui existent entre les molécules (ex : film alimentaire)
elles sont liés aux charges électriques permanentes portées par les atomes des molécules, ou bien aux mouvements désordonnés des électrons à l’intérieur des molécules, qui vont faire apparaitre des charges partielles instantanées. |
5.2 solubilité d'une espèce chimique
une solution est obtenue par dissolution d’un soluté (ionique ou moléculaire) dans un solvant.
une solution est toujours électriquement neutre.
le solvant est l’espèce majoritaire d’une solution.
un solvant constitué de molécules polaires (ex. eau) est un solvant polaire, qui dissoudra les solutés ioniques et les solutés moléculaires polaires (ex. glucose).
un solvant constitué de molécules apolaires (ex. cyclohexane) est un solvant apolaire, qui dissoudra les solutés moléculaires apolaires (ex. huile).
une solution est toujours électriquement neutre.
le solvant est l’espèce majoritaire d’une solution.
un solvant constitué de molécules polaires (ex. eau) est un solvant polaire, qui dissoudra les solutés ioniques et les solutés moléculaires polaires (ex. glucose).
un solvant constitué de molécules apolaires (ex. cyclohexane) est un solvant apolaire, qui dissoudra les solutés moléculaires apolaires (ex. huile).
|
|
|
|
|
|
5.3 solubilité d'une espèce dans un solvant
|
|
|