la molécule d'eau
|
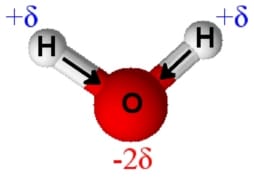
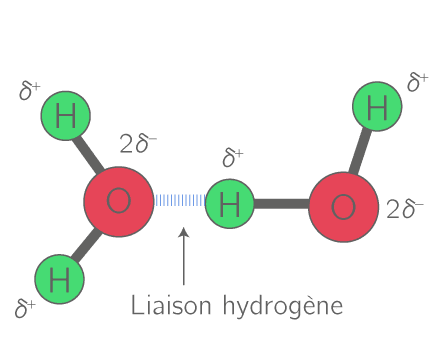
Dans la molécule d’eau, l'oxygène, beaucoup plus électronégatif que l'hydrogène, attire vers lui les électrons mis en commun dans la liaison. La liaison covalente O-H est polarisée.
Cette répartition inégale des électrons confère à l'oxygène une charge partielle négative et à l'hydrogène une charge partielle positive. La lettre grecque delta (δ) indique la présence d'une charge partielle. La molécule d’eau est polaire. |
solubilisation
|
On qualifie d'hydrophiles les substances solubles dans l'eau :
les composés ioniques, et les molécules polaires comme le glucose ou le saccharose (qui est le sucre alimentaire). Des molécules organiques portant des groupes fonctionnels polaires comme les alcools à chaîne courte sont également très solubles dans l'eau. |
Une solution aqueuse est un mélange homogène d'au moins deux substances : l'eau (= solvant, en gros excès) + composés hydrophiles (= soluté).
Les solutions paraissent homogènes au microscope, et le soluté ne peut pas être séparé par filtration. |
|
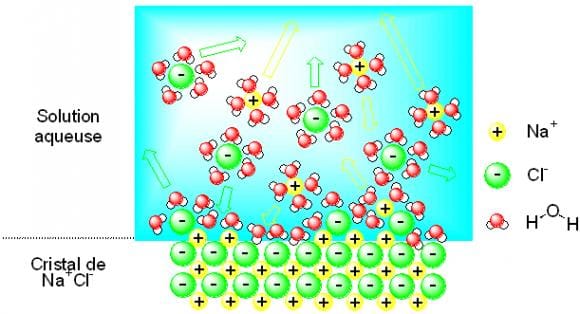
dissolution des solides ioniques :
1 – Dispersion des ions par dislocation du réseau cristallin 2 – Solvatation (= hydratation) par interaction ion-dipôle. D'autant plus forte que l'ion est petit et chargé. Les ions se retrouvent entourés de molécules d'eau, ce qui diminue leur interaction et les éloigne l'un de l'autre. |
|
|
|
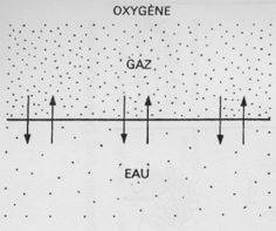
dissolution des gaz
A l’équilibre, la concentration en dioxygène est différente selon le milieu où l’on se situe. Ceci est du à la solubilité du dioxygène qui est différente entre l’eau et l’air.
Dans l’air, la quantité de dioxygène disponible ne dépend pas de la température alors que dans l’eau la concentration en dioxygène est dépendante de la température.
Un animal respirant dans l’eau a peu de dioxygène à sa disposition : en milieu aquatique, les consommations de dioxygène doivent être faibles.
Dans l’air, la quantité de dioxygène disponible ne dépend pas de la température alors que dans l’eau la concentration en dioxygène est dépendante de la température.
Un animal respirant dans l’eau a peu de dioxygène à sa disposition : en milieu aquatique, les consommations de dioxygène doivent être faibles.
Pour ce qui concerne le dioxyde de carbone, les résultats ne sont pas du même genre, les concentrations à l’équilibre sont quasiment les mêmes, que l’on soit dans l’eau ou dans l’air. Le dioxyde de carbone a une solubilité 30 fois supérieure à celle du dioxygène.
Le fait que le dioxyde de carbone soit très soluble et que les poissons soient obligés de brasser beaucoup d’eau pour peu de dioxygène donne un sang artériel très pauvre en dioxyde de carbone ; la régulation du pH plasmatique est donc différente de celle des animaux à respiration aérienne.
Le fait que le dioxyde de carbone soit très soluble et que les poissons soient obligés de brasser beaucoup d’eau pour peu de dioxygène donne un sang artériel très pauvre en dioxyde de carbone ; la régulation du pH plasmatique est donc différente de celle des animaux à respiration aérienne.
Loi de Henry
La solubilité d'un gaz dans l'eau se calcule en exprimant que, lorsque la solution est saturée,
il y a égalité des potentiels chimiques du corps pur concerné dans la phase aqueuse et dans la solution.
Si le gaz est assimilable à un gaz parfait, et si la solution obtenue est diluée et assimilable à une solution parfaite, on a, à l’équilibre, la solubilité massique à saturation : Cs = H × Pgaz
Cs : Concentration en gaz dissous dans la solution à l'équilibre (g/L)
Pgaz : Pression partielle de gaz dans l'air (Pa) ; p(O2) = 21 % Patm ; p(CO2) = 0,03 % Patm ; p(N2) = 79 % Patm
H : Constante de Henry, fonction du gaz et de la température (g.L^-1.Pa^-1), donnée dans des tables.
La solubilité d'un gaz dans l'eau se calcule en exprimant que, lorsque la solution est saturée,
il y a égalité des potentiels chimiques du corps pur concerné dans la phase aqueuse et dans la solution.
Si le gaz est assimilable à un gaz parfait, et si la solution obtenue est diluée et assimilable à une solution parfaite, on a, à l’équilibre, la solubilité massique à saturation : Cs = H × Pgaz
Cs : Concentration en gaz dissous dans la solution à l'équilibre (g/L)
Pgaz : Pression partielle de gaz dans l'air (Pa) ; p(O2) = 21 % Patm ; p(CO2) = 0,03 % Patm ; p(N2) = 79 % Patm
H : Constante de Henry, fonction du gaz et de la température (g.L^-1.Pa^-1), donnée dans des tables.
|
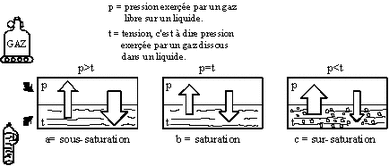
le taux de saturation en gaz se calcule en divisant la concentration mesurée par la concentration à saturation Cs, qui est donnée par des tables (table de Truesdale) ou des formules empiriques.
Si Ts > 100 %, l’eau est sursaturée en gaz. Si Ts < 100 %, l’eau est sous-saturée. |
Dans l’eau à pression atmosphérique normale, la concentration à saturation en oxygène dissous est calculable par la formule suivante : Cs = (475 − 2,65 × S) / (33,5 +θ)
Cs : concentration en O2 à l'équilibre (mg/L) ; S : salinité en g de sel par L (ou ‰) ; θ : température en °C |
|
Paramètres influençant la solubilité
La teneur en gaz dissous dépend de nombreux paramètres : • La nature du gaz (polaire ou non). Ex : H(CO2) = 32 × H(O2). Les gaz toxiques NH3 et H2S sont énormément solubles dans l’eau : il est difficile de les chasser de l’eau. • la vitesse de dilution du gaz • la température T ou θ : si θ ➚, H ➘ donc Cs ➘ • la salinité S : si S ➚, Cs ➘ • l’altitude h : si h ➚, P ➘ donc Cs ➘ • la profondeur z dans l’eau : si z ➚, P ➚ donc Cs ➚ (pression P sous z mètres d’eau = pression hydrostatique : P = ρgz) |