diaporamas illustrés de cours :
- introduction biotopes aquatiques
- lumière / matière
- gaz dissous
- dissolution
- carbonates
- cycle de l'azote
- introduction biotopes aquatiques
- lumière / matière
- gaz dissous
- dissolution
- carbonates
- cycle de l'azote
cycles biogéochimiques : étude du transport et des transformations des substances chimiques (C, N, P, eau, métaux...).
l'eau
Cliquer ici pour modifier.
l'eau et ses propriétés
Cliquer ici pour modifier.
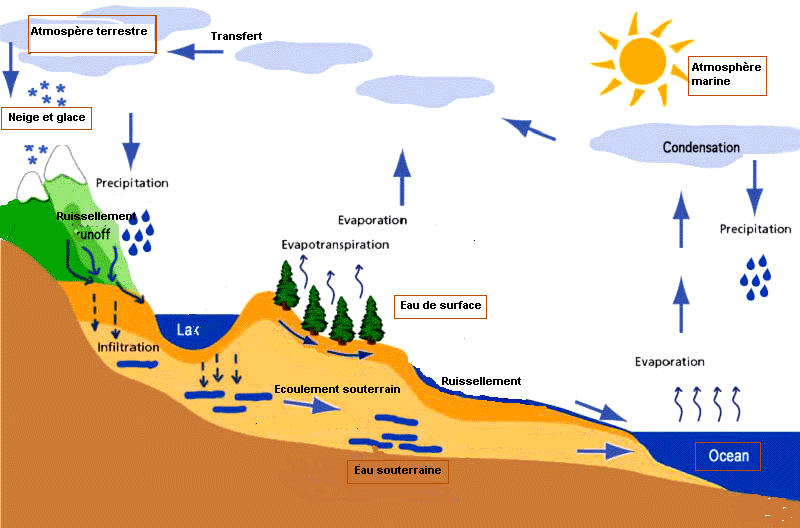
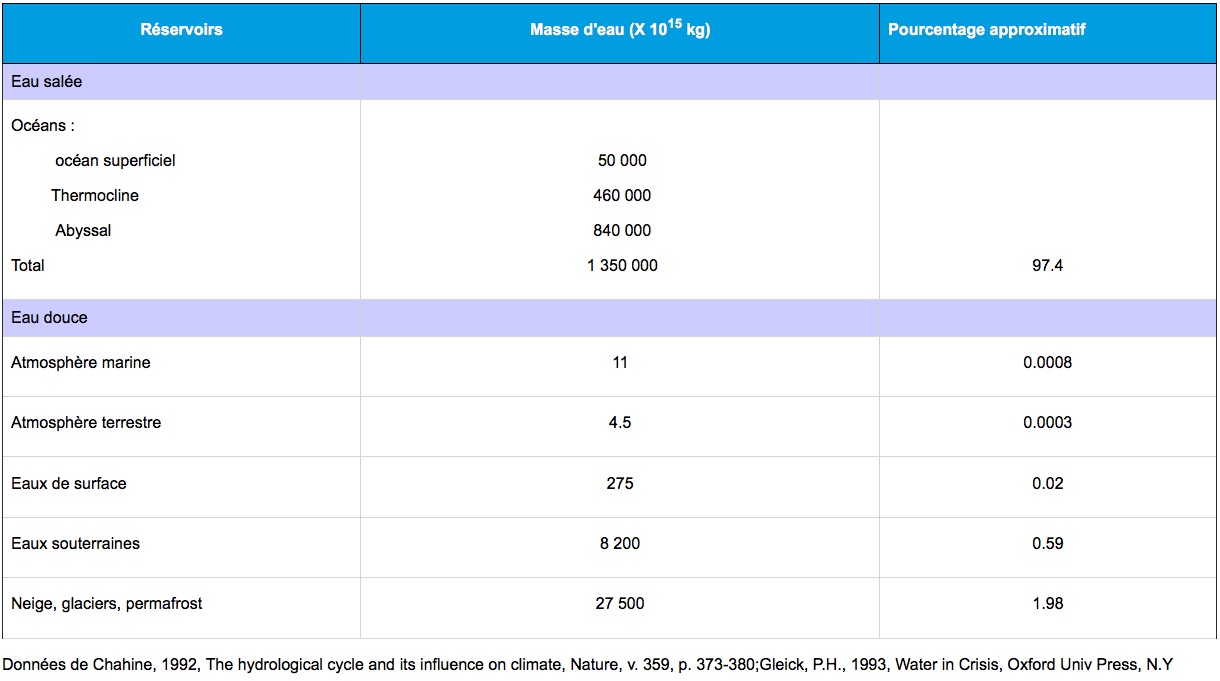
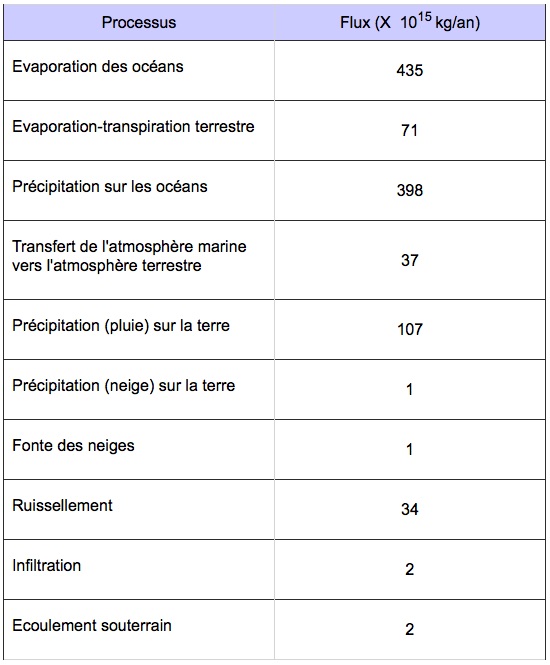
cycle de l'eau
Cliquer ici pour modifier.
substances dissoutes
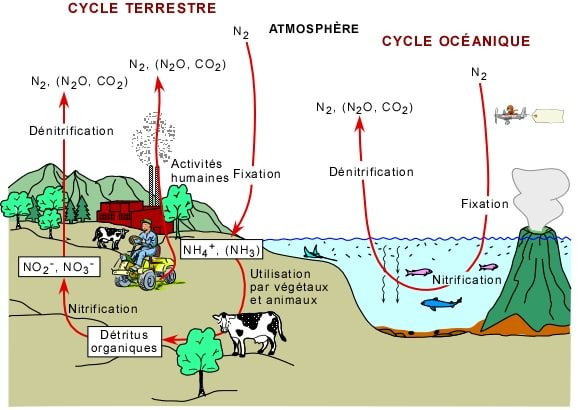
cycle de l'azote
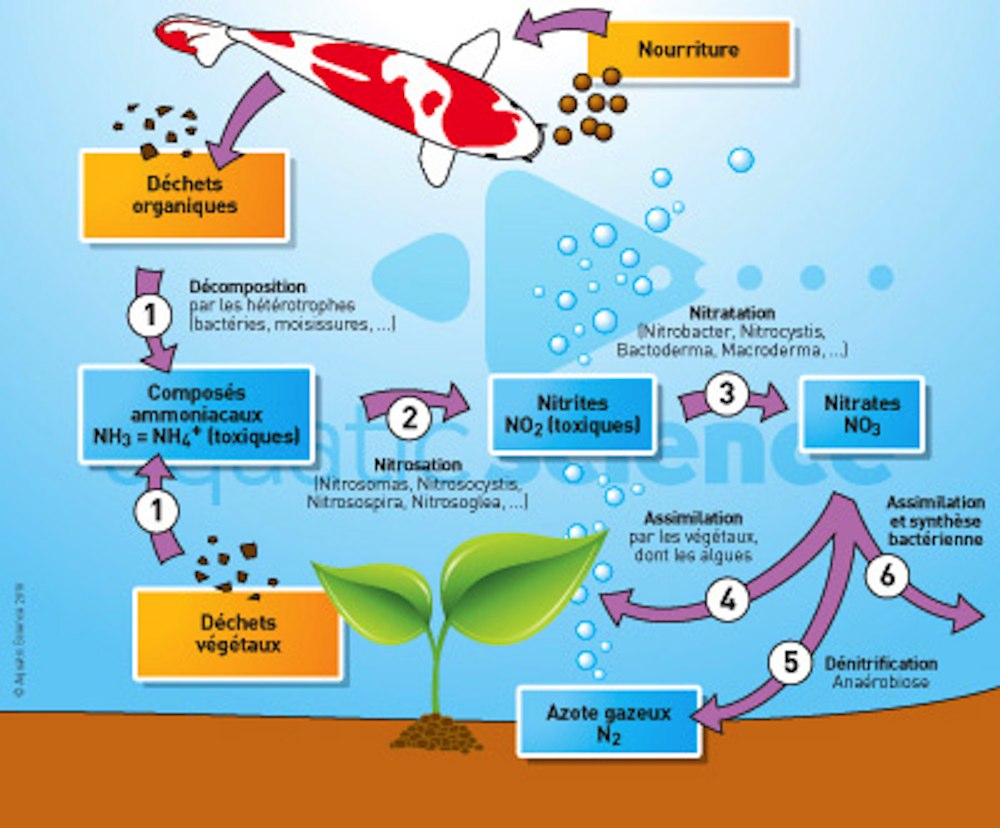
Les animaux rejettent des déchets organiques dans l’eau. À cela s’ajoutent la décomposition des végétaux et du surplus éventuel de nourriture.
|
Ammonisation ou ammonification (décomposition des déchets)
Les déchets organiques présents dans un bassin se décomposent en deux principaux composés azotés en fonction du pH, l’ammonium (NH4+) qui est très peu toxique, et l’ammoniac (NH3), hautement toxique. |
Nitrification (deux phases aérobie) :
Nitrosation : ces composés sont convertis en nitrites (NO2-) par des bactéries dites nitrifiantes appelées nitrosomonas. Ces nitrites sont eux aussi excessivement toxiques pour les poissons. Nitratation : les nitrites sont convertis en nitrates (NO3-) par les bactéries de type nitrobacter. Les nitrates, beaucoup moins toxiques que les autres composés azotés, et très solubles dans l’eau, ne sont dangereux que s’ils sont en trop grande concentration dans l’eau. Cependant ils sont extrêmement toxiques pour les invertébrés marins. Ceux-ci seront en partie assimilés par les plantes comme nutriments (absorption), en partie transformés en azote gazeux N2 (dénitrification) et en protéines. |
phosphore
Le phosphore joue un rôle essentiel dans de nombreuses molécules de la matière vivante :
il est associé à des combinaisons organiques multiples, dans les acides nucléiques, les ADN et ARN dont il constitue le squelette ainsi qu'à de nombreux protides et lipides qu'on qualifie de phosphoprotéines et de phospholipides.
Il est le composant central de l'ATP (adénosine triphosphorique) producteur d'énergie.
Il intervient dans la photosynthèse.
il est associé à des combinaisons organiques multiples, dans les acides nucléiques, les ADN et ARN dont il constitue le squelette ainsi qu'à de nombreux protides et lipides qu'on qualifie de phosphoprotéines et de phospholipides.
Il est le composant central de l'ATP (adénosine triphosphorique) producteur d'énergie.
Il intervient dans la photosynthèse.
|
Pratiquement tout le phosphore en milieu terrestre est dérivé de l’altération des phosphates de calcium des roches de surface, principalement de l’apatite. Bien que les sols contiennent un grand volume de phosphore, une petite partie seulement est accessible aux organismes vivants. Ce phosphore est absorbé par les plantes et transféré aux animaux par leur alimentation. Une partie est retournée aux sols à partir des excréments des animaux et de la matière organique morte. Une autre partie est transportée vers les océans où une fraction est utilisée par les organismes benthiques et ceux du plancton pour secréter leur squelette; l’autre fraction se dépose au fond de l’océan sous forme d’organismes morts ou de particules et est intégrée aux sédiments. Ces derniers sont transformés progressivement en roches sédimentaires par l’enfouissement; beaucoup plus tard, les roches sont ramenées à la surface par les mouvements tectoniques et le cycle recommence.
|
rôle fertilisant du phosphore :
une fois les réserves des graines épuisées en phosphore, les plantes doivent trouver cet élément dans le sol à proximité de leurs racines, puisque cet élément n'est pratiquement pas mobile. A ce stade, le phosphore peut s'avérer un facteur limitant majeur et entraîner un retard de croissance et de développement. L'apport de phosphore au semis favorise la vigueur au démarrage et stimule la croissance du système racinaire qui va plus rapidement explorer les réserves en phosphore du sol. L’activité humaine intervient dans le cycle du phosphore en exploitant des mines de phosphate, en grande partie pour la fabrication des fertilisants. Ajoutés aux sols en excès, les phosphates sont drainés vers les systèmes aquatiques. Puisque le phosphore est souvent un nutriment limitatif dans les rivières, les lacs et les eaux marines côtières, une addition de phosphore dans ces systèmes peut agir comme fertilisant et générer des problèmes d’eutrophisation (forte productivité biologique résultant d’un excès de nutriments).
|
carbone
Les réservoirs à court terme se trouvent dans la végétation terrestre et marine, les animaux terrestres et marins, dans le CO2 atmosphérique et dissous dans les couches supérieurs de l’océan.
Cliquer ici pour modifier.
oxygène
Cliquer ici pour modifier.
matière organique
Cliquer ici pour modifier.
ressources internet
eaufrance : le portail eaufrance est le point d’accès unique à toutes les informations et les données publiques relatives à l’eau et aux milieux aquatiques. Exemples :
- zones-humides : ce site présente les milieux humides et dresse un panorama des fonctions, des menaces et de la réglementation qui s’y applique. Il apporte également des informations sur les outils et structures compétentes pour mener des actions de préservation et de restauration.
- data : Ce site offre un accès libre aux données sur l'eau, les milieux aquatiques et leurs usages, publiées sur les sites de la toile Eaufrance.
|
|
|
bibliographie
|
résumé
L'eau est aussi bien une originalité physique, une curiosité chimique et par là même un véhicule de pollution, mais aussi une richesse et donc un enjeu économique. Le présent ouvrage aborde ces quatre points, du point de vue du physico-chimiste, avec des ouvertures sur la physique, la géologie ou la biologie. Il ne s'agit ni d'un livre de cours de chimie, ni d'un article de revue pour un journal scientifique, mais d'un fascicule qui, partant de la très spéciale molécule d'eau, dont les propriétés fondamentales en physico-chimie sont résumées, montre que la physico-chimie est une science conduisant à de nombreuses applications pratiques dont l'importance est fondamentale sur le plan économique. Cet ouvrage est d'un niveau très accessible, allant des élèves des classes de lycée, voulant comprendre le monde environnant, aux professeurs, en passant par un public curieux scientifiquement qui s'interroge sur le pourquoi des choses. Nous espérons que cet opuscule fera percevoir au lecteur le vaste domaine d'intervention de la chimie et lui fera prendre conscience de l'intérêt pratique de notions rencontrées dans un cours académique. CDI : 546.22 SIG ; 2014
résumé
La chimie des milieux aquatiques étudie la nature des substances dissoutes et en suspension dans les eaux naturelles et autres systèmes aquatiques, ainsi que les équilibres chimiques et les processus physico-chimiques dans lesquels ces substances sont impliquées. Cette discipline tient aussi compte des processus biologiques, géochimiques et physiques dans ces milieux. Cette cinquième édition a été entièrement révisée pour tenir compte des nouvelles avancées scientifiques et techniques d'analyse ainsi que de la chimie des milieux aquatiques. Sont ainsi abordés les nouveaux procédés de traitement de l'eau potable, le cycle du fer et son rôle comme nutriment dans les océans, les nanoparticules manufacturées, les xénobiotiques. De nombreux exemples et des exercices corrigés illustrent les principes exposés. Des compléments (données thermodynamiques) sont accessibles sur le site dunod.com. |
CDI : 546.22 MIC ; 2002
résumé
L'eau est le principal réactif utilisé dons cette grande usine chimique qu'est la terre. Les eaux naturelles constituent un immense champ d'application de la théorie des équilibres en solution aqueuse. Beaucoup de réactions en milieu naturel atteignent l'équilibre, en particulier les réactions acide-base, dont on montrera l'importance dominante. Une grande partie de cet ouvrage est destinée à montrer comment les notions d'équilibre introduites en chimie des solutions peuvent être étendues et former la base de la géochimie des eaux. La connaissance des équilibres permet aussi de mettre en évidence l'existence de déséquilibres en particulier pour les réactions avec changement de phase (transfert entre eau et atmosphère, dissolution et formation des minéraux des roches) et pour les réactions d'oxydo-réduction, qui dons la nature sont en relation étroite avec les processus biologiques. Ces réactions doivent être abordées sous l'ongle cinétique mois les résultats des études cinétiques de laboratoire s'appliquent mal aux milieux naturels. On présentera quelques exemples d'étude de cinétique globale de systèmes aqueux naturels utilisant comme chronomètre des isotopes radioactifs. L'étude de quelques systèmes aquatiques naturels : eaux thermales, lacs et océans donne l'occasion d'appliquer les connaissances théoriques développées dans les premiers chapitres. L'ouvrage est principalement destiné aux étudiants de Licence et de Maîtrise de Sciences de la Terre, de Chimie et d'Etude en Environnement. La théorie est limitée à l'indispensable, les traitements graphiques sont fortement développés et des exercices, avec corrigés détaillés, devraient entraîner à la résolution des problèmes pratiques. Le livre peut également être utile pour rappeler les principes de base aux chercheurs et ingénieurs travaillant dons le vaste domaine des Sciences de l'Eau, domaine dont l'importance ne fera que croître. |